CAPA là gì? Các bước thực hiện CAPA cho ngành Dược
20:14 - 19/09/2024 2595
Tiêu chuẩn EN 1822 đối với bộ lọc Hepa H13, H14, ULPA U15
Yêu Cầu Đối Với Thiết Bị Phòng Sạch Đạt Tiêu Chuẩn GMP EU
Hướng Dẫn Thiết Kế Phòng Sạch Đạt Chuẩn ISO Class 5
Tiêu chuẩn EU-GMP và sự khác biệt với tiêu chuẩn WHO-GMP
CAPA (Corrective and Preventive Actions) là một quy trình quản lý chất lượng quan trọng trong ngành Dược, nhằm đảm bảo rằng các vấn đề liên quan đến sản phẩm, quy trình sản xuất hoặc hệ thống chất lượng được xác định, phân tích, và giải quyết một cách hiệu quả. CAPA giúp ngăn ngừa tái diễn các sai sót trong quá trình sản xuất và cải tiến hệ thống quản lý chất lượng. Trong bối cảnh ngành Dược yêu cầu nghiêm ngặt về an toàn và hiệu quả của sản phẩm, việc thực hiện CAPA chính xác là rất quan trọng.
CAPA là gì?
CAPA là viết tắt của "Corrective and Preventive Actions", tạm dịch là "Hành động khắc phục và phòng ngừa". Đây là một quy trình hệ thống nhằm:
- Hành động khắc phục (Corrective Action): Khắc phục nguyên nhân gốc rễ của các sự cố hoặc vấn đề đã xảy ra.
- Hành động phòng ngừa (Preventive Action): Ngăn ngừa các vấn đề hoặc sai sót tiềm ẩn xảy ra trong tương lai.
Trong ngành Dược, CAPA được thực hiện để đáp ứng yêu cầu của các quy định như Good Manufacturing Practices (GMP) hoặc Good Distribution Practices (GDP), nhằm đảm bảo sản phẩm được sản xuất và phân phối an toàn, hiệu quả và phù hợp với các tiêu chuẩn chất lượng.
Tầm quan trọng của CAPA trong ngành Dược
Ngành Dược đòi hỏi sự nghiêm ngặt về chất lượng sản phẩm, vì bất kỳ sai sót nào cũng có thể ảnh hưởng nghiêm trọng đến sức khỏe người tiêu dùng. Do đó, CAPA đóng vai trò rất quan trọng trong:
- Đảm bảo tuân thủ quy định: Các cơ quan như FDA hoặc EMA yêu cầu các công ty dược phải thực hiện CAPA khi phát hiện các vấn đề liên quan đến sản phẩm hoặc quy trình.
- Ngăn ngừa tái diễn sự cố: CAPA giúp xác định và xử lý nguyên nhân gốc rễ của vấn đề, từ đó ngăn ngừa việc xảy ra sai sót tương tự.
- Cải thiện hiệu quả hoạt động: CAPA không chỉ giúp khắc phục vấn đề hiện tại mà còn giúp nâng cao hiệu quả và độ tin cậy của quy trình sản xuất.
Các phần của CAPA
CAPA (Corrective and Preventive Actions) bao gồm hai phần chính: Hành động khắc phục (Corrective Action) và Hành động phòng ngừa (Preventive Action). Dưới đây là chi tiết về từng phần cũng như các bước triển khai từng phần trong CAPA.
1. Hành động khắc phục (Corrective Action)
Hành động khắc phục tập trung vào việc sửa chữa và loại bỏ nguyên nhân gốc rễ của một vấn đề đã xảy ra. Mục tiêu là đảm bảo rằng vấn đề sẽ không tái diễn trong tương lai. Quy trình khắc phục thường bao gồm các bước sau:
a) Xác định vấn đề
- Nguồn vấn đề: Có thể đến từ các báo cáo khiếu nại của khách hàng, lỗi phát hiện trong quy trình sản xuất, hay trong các cuộc kiểm tra chất lượng.
- Mô tả vấn đề: Xác định và mô tả chi tiết vấn đề đã xảy ra, phạm vi ảnh hưởng và các yếu tố liên quan.
b) Phân tích nguyên nhân gốc rễ
- Điều tra sâu: Sử dụng các công cụ như 5 Why Analysis hoặc Fishbone Diagram để xác định nguyên nhân cốt lõi.
- Dữ liệu phân tích: Sử dụng dữ liệu từ quy trình sản xuất, báo cáo kỹ thuật hoặc kết quả thử nghiệm để hỗ trợ quá trình phân tích.
c) Đề xuất giải pháp khắc phục
- Sau khi xác định nguyên nhân, đề xuất các biện pháp cụ thể để sửa chữa vấn đề. Ví dụ, có thể là sửa đổi quy trình, cập nhật tài liệu kỹ thuật hoặc thay thế thiết bị lỗi.
d) Thực hiện hành động khắc phục
- Triển khai các giải pháp đã đề xuất, đảm bảo rằng chúng được thực hiện kịp thời và đầy đủ.
e) Đánh giá và theo dõi
- Theo dõi hiệu quả: Sau khi thực hiện, cần theo dõi kết quả để đảm bảo vấn đề đã được giải quyết hoàn toàn.
- Đánh giá lại: Nếu vấn đề vẫn còn, cần phân tích lại và thực hiện các hành động bổ sung.
2. Hành động phòng ngừa (Preventive Action)
Hành động phòng ngừa nhằm ngăn chặn các vấn đề hoặc sự cố có thể xảy ra trong tương lai. Mục tiêu của phần này là dự đoán và loại bỏ các yếu tố tiềm ẩn gây lỗi trước khi chúng phát sinh.
a) Xác định các nguy cơ tiềm ẩn
- Phân tích dữ liệu: Dựa trên kết quả phân tích từ các cuộc kiểm toán, kiểm tra định kỳ hoặc phản hồi từ khách hàng, để nhận diện các nguy cơ có thể xảy ra.
- Đánh giá hệ thống: Xem xét các quy trình và hệ thống đang hoạt động để xác định các điểm yếu hoặc lỗ hổng.
b) Phân tích nguy cơ
- Xác định mức độ nghiêm trọng và khả năng xảy ra của các nguy cơ đã được phát hiện. Điều này giúp xác định được những vấn đề cần ưu tiên xử lý.
c) Đề xuất hành động phòng ngừa
- Đề xuất các biện pháp nhằm ngăn chặn nguy cơ trước khi chúng trở thành vấn đề. Ví dụ: cập nhật quy trình làm việc, cải tiến hệ thống quản lý chất lượng hoặc đào tạo lại nhân viên.
d) Thực hiện hành động phòng ngừa
- Thực hiện các biện pháp phòng ngừa để giảm thiểu hoặc loại bỏ nguy cơ tiềm ẩn. Đảm bảo các thay đổi này được áp dụng đúng cách và toàn diện.
e) Theo dõi và đánh giá
- Theo dõi quá trình triển khai các hành động phòng ngừa để đảm bảo rằng chúng thực sự hiệu quả. Điều này bao gồm việc kiểm tra thường xuyên và điều chỉnh các biện pháp khi cần thiết.
3. Tài liệu và báo cáo
Mọi quy trình trong CAPA, từ xác định vấn đề, phân tích nguyên nhân đến thực hiện và đánh giá hành động, đều cần được ghi lại đầy đủ và chính xác. Đây là một yêu cầu quan trọng trong việc tuân thủ các quy định của cơ quan quản lý như FDA, EMA hoặc các tiêu chuẩn phòng sạch Good Manufacturing Practices (GMP).
a) Lập hồ sơ CAPA
- Mọi hoạt động trong quá trình thực hiện CAPA cần được ghi chép cẩn thận, từ việc phát hiện vấn đề cho đến các hành động khắc phục và phòng ngừa.
b) Báo cáo kiểm toán
- Báo cáo này giúp chuẩn bị cho các cuộc kiểm toán nội bộ hoặc từ các cơ quan quản lý. Hệ thống tài liệu đầy đủ cũng giúp theo dõi và đánh giá hiệu quả của quá trình CAPA trong tương lai.
Các bước thực hiện CAPA trong ngành Dược
>> Xem thêm: Công nghệ nào sẽ được lựa chọn trong xét nghiệm vô trùng?
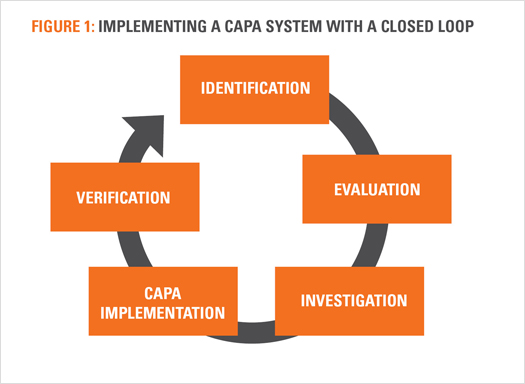
Thực hiện quy trình CAPA hiệu quả đòi hỏi phải tuân thủ một số bước cơ bản sau:
Bước 1: Xác định vấn đề
Quá trình CAPA bắt đầu bằng việc xác định vấn đề. Các vấn đề có thể phát sinh từ nhiều nguồn khác nhau, bao gồm các khiếu nại từ khách hàng, kết quả kiểm tra chất lượng, hoặc các báo cáo từ các cuộc kiểm toán nội bộ hoặc bên ngoài.
Bước 2: Phân tích nguyên nhân gốc rễ
Sau khi xác định vấn đề, việc quan trọng là phân tích nguyên nhân gốc rễ. Đây là quá trình điều tra để tìm ra lý do thực sự khiến vấn đề xảy ra. Các công cụ như Fishbone Diagram (biểu đồ xương cá) hoặc 5 Why Analysis (phân tích 5 câu hỏi “Tại sao”) thường được sử dụng để tìm ra nguyên nhân cốt lõi.
Bước 3: Đề xuất hành động khắc phục
Sau khi xác định nguyên nhân, các hành động khắc phục cần được đề xuất. Các biện pháp này tập trung vào việc sửa chữa vấn đề đã xảy ra và đảm bảo rằng nó sẽ không tái diễn. Các biện pháp khắc phục có thể liên quan đến việc thay đổi quy trình sản xuất, đào tạo lại nhân viên, hoặc cải tiến các hệ thống quản lý chất lượng.
Bước 4: Thực hiện hành động phòng ngừa
Hành động phòng ngừa tập trung vào việc ngăn ngừa các sự cố tương tự có thể xảy ra trong tương lai. Điều này bao gồm việc đánh giá toàn bộ hệ thống và quy trình để phát hiện các lỗ hổng tiềm ẩn và sửa đổi chúng trước khi sự cố xảy ra.
Bước 5: Đánh giá hiệu quả
Sau khi các hành động khắc phục và phòng ngừa được thực hiện, cần phải đánh giá hiệu quả của chúng. Điều này đòi hỏi phải theo dõi các kết quả và đảm bảo rằng các vấn đề không tái diễn, đồng thời đảm bảo rằng quy trình quản lý chất lượng đã được cải tiến.
Bước 6: Lập hồ sơ và báo cáo
Mọi hành động trong quá trình CAPA cần được ghi nhận đầy đủ và lưu trữ trong hồ sơ. Việc lập hồ sơ không chỉ giúp theo dõi quá trình mà còn là yêu cầu bắt buộc của các cơ quan quản lý. Báo cáo CAPA thường được trình bày trong các cuộc kiểm toán hoặc khi có yêu cầu từ cơ quan quản lý.
Những thách thức trong thực hiện CAPA
- Xác định đúng nguyên nhân gốc rễ: Đôi khi việc xác định nguyên nhân gốc rễ là một quá trình phức tạp và đòi hỏi sự hợp tác từ nhiều bộ phận.
- Nguồn lực hạn chế: Thực hiện CAPA yêu cầu sự đầu tư về thời gian, công sức và tài chính, đôi khi có thể gây khó khăn cho doanh nghiệp.
- Theo dõi và đánh giá hiệu quả: Đảm bảo rằng các biện pháp CAPA mang lại hiệu quả lâu dài có thể là một thách thức.
Kết luận
CAPA là một quy trình không thể thiếu trong ngành Dược, giúp đảm bảo rằng các vấn đề về chất lượng và an toàn sản phẩm được giải quyết triệt để. Với một quy trình CAPA hiệu quả, doanh nghiệp không chỉ đảm bảo tuân thủ các quy định của pháp luật mà còn nâng cao chất lượng sản phẩm, tạo niềm tin với người tiêu dùng và bảo vệ sức khỏe cộng đồng.
Thông tin chi tiết về TƯ VẤN - THIẾT KẾ - THI CÔNG PHÒNG SẠCH, vui lòng liên hệ:
 | Công ty Cổ phần Cơ điện Phòng sạch Anh Khang Hotline: 1900 636 814 Email: info@akme.com.vn Website: akme.com.vn Add: Lô B7 Xuân Phương Garden, Đường Trịnh Văn Bô, Phường Phương Canh, Quận Nam Từ Liêm, Hà Nội. |
12:05 - 28/11/2019 48413
THIẾT KẾ VÀ THI CÔNG PHÒNG SẠCH
14:05 - 11/03/2025 23968
Thi Công Phòng Sạch
14:18 - 11/03/2025 12763
Thi Công Phòng Sạch Y Tế
14:13 - 28/02/2025 24138
Thi Công Phòng Sạch Điện Tử
16:15 - 18/03/2021 6857
DỊCH VỤ BẢO HÀNH
16:26 - 28/11/2019 19970
CUNG CẤP, LẮP ĐẶT THIẾT BỊ PHÒNG SẠCH
14:50 - 26/11/2019 6580
TƯ VẤN DÂY CHUYỀN CÔNG NGHỆ
16:35 - 19/03/2025 20277